Presentan plan para biotecnológicos biosimilares
- Escrito por Redacción
- Publicado en Bienestar 24 horas
- 0 comentarios
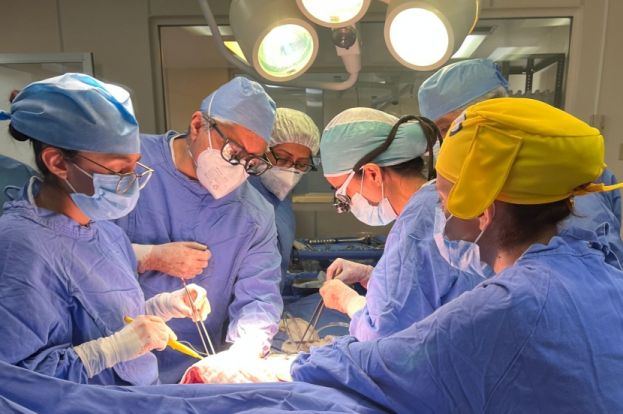
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris), presentó la Estrategia de Certidumbre Regulatoria para el Sector Farmacéutico: Biosimilares, que tiene por objetivo consolidar un marco regulatorio y operativo que respalde y fortalezca la producción y desarrollo de medicamentos biotecnológicos biosimilares.
Este esfuerzo contempla un plan de trabajo de cuatro años, con acciones inmediatas, y a corto y mediano plazo, considerando todo el ciclo de vida del producto farmacéutico.
Alejandro Svarch Pérez, titular del organismo, explicó que se logrará el impulso, asesoramiento y fortalecimiento de la producción nacional de medicamentos biosimilares e innovadores, para lo cual es necesario establecer políticas públicas enfocadas que fomenten la industria local de biotecnológicos, teniendo en cuenta tres aspectos clave.
También puedes leer. Aprueba Cofepris nuevo medicamentos. https://revistafactorrh.com/bienestar-24-horas/item/10978-aprueba-cofepris-nuevos-medicamentos
“Primero, impulsar el desarrollo de medicamentos biotecnológicos biocomparables, que deriven en alternativas terapéuticas elaboradas por y para el pueblo de México, contribuyendo así a la autosuficiencia tecnológica. Segundo, establecer un marco institucional y regulatorio robusto, alineado a estándares internacionales, que proporcione certidumbre regulatoria a los fabricantes establecidos en México y garantice la calidad, seguridad y eficacia de estos medicamentos. Y tercero, fomentar la capacidad de la industria, mediante estrategias específicas de acompañamiento regulatorio en todas las fases de investigación y producción del producto farmacéutico.”
El plan de trabajo para poner en marcha esta estrategia de certidumbre regulatoria incluye la creación de un grupo específico dentro del Comité de Buenas Prácticas Regulatorias, así como la Unidad Especializada en Medicamentos Biotecnológicos Biosimilares (UEBio), conformada por un equipo interdisciplinar con personal experto de Cofepris, que será clave para agilizar la mejora regulatoria y supervisar los medicamentos biocomparables, acabando con la fragmentación actual de procesos.