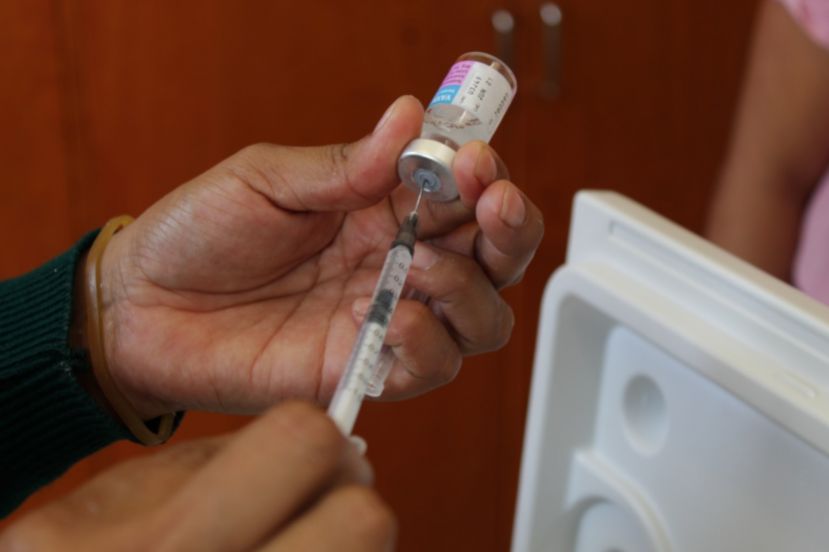
Dan revés a vacuna de AstraZeneca
- Escrito por Redacción
- Publicado en Bienestar 24 horas
- 0 comentarios
La Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) informó que el Comité de Moléculas Nuevas (CMN) evaluó la información técnica y científica proporcionada por AstraZeneca en relación con su vacuna contra el virus SARS-CoV-2, y emitió por unanimidad una opinión no favorable.
Durante el análisis de los datos presentados por el fabricante sobre la vacuna Vaxzevria ChAdOx-1-S de tipo recombinante, los expertos del CMN confirmaron su seguridad; sin embargo, determinaron que se deberá presentar información actualizada sobre su eficacia e inmunogenicidad para poder avanzar en el proceso hacia la autorización del registro sanitario.
Los expertos hicieron mención de que AstraZeneca no presentó datos sobre las variantes que circulan actualmente en México y a nivel global. Asimismo, coincidieron en que, si bien existe amplia evidencia de la seguridad de este biológico en el país, es importante conocer información más detallada sobre su farmacovigilancia en México, principalmente sobre eventos adversos específicos, además de que los representantes del fabricante no brindaron una respuesta convincente sobre el beneficio que esta vacuna puede tener en poblaciones vulnerables.
También puedes leer. Avalan vacuna de Pfizer. https://revistafactorrh.com/bienestar-24-horas/item/10380-dan-aval-a-vacuna-de-pfizer-para-ser-comercializada
El CMN determinó que el solicitante no reportó la actualización de cepas; no presentó datos suficientes de inmunogenicidad y no se sustentó el beneficio de esta vacuna en condiciones de vulnerabilidad como inmunodeficiencias primarias y adquiridas.
Aunque las sesiones del CMN no son públicas, en cumplimiento al compromiso de total transparencia, por primera vez la población conoce en vivo las deliberaciones sobre la información técnica y científica de las vacunas contra el SARS-CoV 2.
Cabe destacar que AstraZeneca podrá volver a presentar la solicitud para la obtención de registro sanitario ante el CMN. Durante la nueva sesión se llevaría a cabo un resumen de las observaciones anteriores y la evaluación se enfocará en su cumplimiento.
Todos los productos que tienen autorización de uso de emergencia, como vacunas y medicamentos, deben continuar con la estructuración de su dossier, incorporando información útil, así como documentación completa para comprobar ante esta autoridad regulatoria que el producto cumple los estándares legales, administrativos y científicos para obtener el registro sanitario.